“美國FDA對(duì)國外藥物進(jìn)入本土市場(chǎng)的監(jiān)管重視程度有增無減,是否可以免除I期、II期臨床取決于研究數(shù)據(jù)質(zhì)量、產(chǎn)品的安全性和臨床數(shù)據(jù)過硬。康柏西普獲得美國FDA批準(zhǔn),直接進(jìn)入III期,說明已經(jīng)具備了完整的藥物有效性和安全性數(shù)據(jù)。”
——前美國FDA高級(jí)評(píng)審官魏曉雄博士表示
近日康弘藥業(yè)研發(fā)的朗沐(康柏西普眼用注射液)獲準(zhǔn)在美國開展III期臨床試驗(yàn),引發(fā)行業(yè)對(duì)于中國創(chuàng)新醫(yī)藥的討論。究竟直接進(jìn)入美國FDA(食品藥品監(jiān)督管理局)III期臨床意味著什么?中國醫(yī)藥企業(yè)在通向FDA的道路上又“遭遇”著怎樣的嚴(yán)苛考驗(yàn)?
全球“通關(guān)”名額不足20個(gè)
統(tǒng)計(jì)數(shù)據(jù)顯示,通過FDA認(rèn)證的新藥,平均開發(fā)成本是10億美元,耗時(shí)10年以上,成功的概率大約是1/6000。
放眼國內(nèi),通過美國食品與藥品監(jiān)督管理局(FDA)審批并由此進(jìn)軍世界主流醫(yī)藥市場(chǎng)一直是中國醫(yī)藥企業(yè)的目標(biāo)和夢(mèng)想,藥品通過FDA上市是一個(gè)極其嚴(yán)格的過程,每年美國FDA批準(zhǔn)上市的新藥不超過20個(gè),能夠直接進(jìn)入臨床III期者,放眼世界寥寥無幾。
因此,將康弘朗沐的“連跳兩級(jí)” 斬獲“FDA III期批準(zhǔn)手續(xù)”稱為中國制藥史上里程碑式的勝利,絕非過譽(yù)。
解讀康柏西普“連跳兩級(jí)”
康柏西普創(chuàng)造的奇跡在于,由于其設(shè)計(jì)、研發(fā)、生產(chǎn),研究的最高質(zhì)量標(biāo)準(zhǔn),不需要在美進(jìn)行I期、II期的臨床試驗(yàn),直接進(jìn)入III期臨床,這對(duì)中國原研的創(chuàng)新藥物國際化之路,將是歷史性的時(shí)刻。
朗沐(康柏西普)是中國醫(yī)藥工業(yè)歷史上第一個(gè)直接進(jìn)入美國FDAIII期臨床研究的創(chuàng)新藥,也是中國第一個(gè)獲得FDA臨床批件(IND)的中國生物藥。朗沐,堪稱國家重大創(chuàng)制專項(xiàng)標(biāo)識(shí)化成果之一。
此次跳級(jí),康弘朗沐(康柏西普)將有望更加快速的進(jìn)入世界醫(yī)藥第一大市場(chǎng)——美國,進(jìn)而更廣闊的天地,在全球范圍內(nèi)改變跨國公司壟斷濕性年齡相關(guān)性黃斑變性(wAMD)治療的格局。
當(dāng)美國人選擇中國創(chuàng)造,你的選擇是什么?
“洋藥”、“國藥”的觀念之爭持續(xù)多年,創(chuàng)新和質(zhì)量標(biāo)準(zhǔn)一度讓“洋藥”引以為傲,“國藥”真的不及“洋藥”嗎?對(duì)于國藥與洋藥的PK,四川的李成(化名)先生有著切身體會(huì),一年前在得知患有后,李成第一時(shí)間到美國進(jìn)行治療,多次赴美踏破鐵鞋而收效甚微,經(jīng)過多方咨詢,最終在國內(nèi)華西醫(yī)院專家的推薦下,使用康柏西普(朗沐)得到了更經(jīng)濟(jì)、有效的治療。
還有一個(gè)患者,來自海外的Aaron(化名)在充分了解病癥治療方案后,不遠(yuǎn)萬里來到中國,選擇用康柏西普治療眼底黃斑水腫(如圖)。如同Aaron選擇康柏西普,未來的國際市場(chǎng)上會(huì)有更多的人選擇“中國創(chuàng)造”。
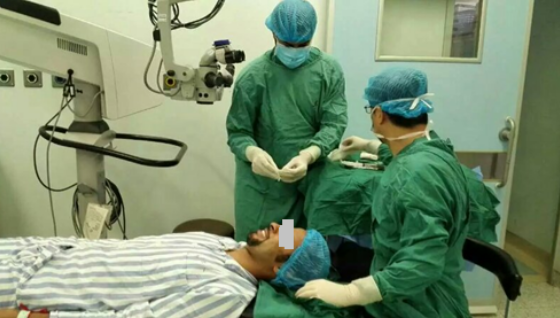
對(duì)于國人而言,此次美國FDA批準(zhǔn)康弘朗沐“連跳兩級(jí)”,是對(duì)國藥創(chuàng)新能力、技術(shù)領(lǐng)先水平極有力的證明,在眼科領(lǐng)域黃斑變性的治療上,國人可以不再“崇洋”。
醫(yī)藥界的“十年一劍”
中國“制造大國”現(xiàn)象的一大憾事,在于眾多企業(yè)放棄對(duì)“至精至微”的追求,“十年磨一劍”的軼事逐漸久遠(yuǎn)。
然而探尋康弘朗沐的成功之路發(fā)現(xiàn),十年前康弘藥業(yè)朗沐(康柏西普)啟動(dòng)研發(fā),累計(jì)投入超10億,同時(shí)將國際最高質(zhì)量標(biāo)準(zhǔn)的要求貫穿從研發(fā)到生產(chǎn)到上市銷售的每一個(gè)環(huán)節(jié)。朗沐的研發(fā)陣容采用國際專家聯(lián)合中國專家的實(shí)力組合,上市兩年時(shí)間,迅速得到市場(chǎng)的廣泛認(rèn)可,在國內(nèi)市場(chǎng)率先打破跨國企業(yè)的強(qiáng)勢(shì)壟斷。
同時(shí),朗沐的國際化之路自它誕生之時(shí)便開始了,回顧上市以來,多項(xiàng)康柏西普的臨床研究結(jié)果,先后被第12屆美國新生血管年會(huì)、2015美國眼科年會(huì)、2015年美國視網(wǎng)膜專家學(xué)會(huì)年會(huì)等全球性的眼科會(huì)議邀請(qǐng)做專題報(bào)道,為朗沐在國際市場(chǎng)上建立了良好的口碑和信譽(yù)。
中國加入WTO組織已經(jīng)十余年,對(duì)于入世影響最大的三個(gè)產(chǎn)業(yè)之一的醫(yī)藥行業(yè),同各國高手在一個(gè)競(jìng)爭平臺(tái)上同舞了十余年。而今,在康弘朗沐這一民族品牌上,我們終于可以調(diào)轉(zhuǎn)觀念,見證創(chuàng)新藥“中國創(chuàng)造”的國際風(fēng)采!
題-1.png)